| Тетраоксид диазота | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
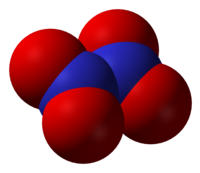
Тетраоксид диазота |
| Сокращения | АТ |
| Традиционные названия | азотный тетраоксид |
| Хим. формула | N2O4 |
| Физические свойства | |
| Состояние | газ (бесцветный) |
| Молярная масса | 92,011 г/моль |
| Плотность | 1,443 г/см³ |
| Термические свойства | |
| Т. плав. | −11,2 °C |
| Т. кип. | +21,1 °C |
| Т. всп. | не горюч °C |
| Энтальпия образования | 9,16 кДж/моль |
| Давление пара | 96 кПа (+20 °C) |
| Химические свойства | |
| Растворимость в воде | реагирует с водой |
| Оптические свойства | |
| Показатель преломления | 1,0012 |
| Структура | |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 10544-72-6 |
| PubChem | 25352 |
| Рег. номер EINECS | 234-126-4 |
| SMILES | |
| InChI | |
| Рег. номер EC | 007-002-00-0 |
| RTECS | QW9800000 |
| ChEBI | 29803 |
| Номер ООН | 1067 |
| ChemSpider | 23681 |
| Безопасность | |
| Токсичность | очень токсичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тетраоксид диазота (азотный тетраоксид, АТ, «амил»[1]) — вещество с формулой N2O4, преобладающее в жидкости, полученной охлаждением диоксида азота ниже точки кипения. Это теоретически бесцветная, но на практике окрашенная в жёлто-коричневый цвет (обусловленный примесью мономерного диоксида азота) летучая ядовитая жидкость с едким запахом. Температура кипения при атмосферном давлении +21,15 °C, кристаллизации — −11 °C. В кристаллическом виде при температурах ниже −12 °C бесцветен.
Свойства [2]

В жидкой и газообразной фазах тетраоксид азота находится в равновесии с диоксидом азота:
при нагревании полностью диссоциирует до диоксида азота. Состав смеси зависит от температуры и давления. С увеличением температуры равновесие смещается в сторону диоксида азота, при этом сжиженный N2O4 окрашивается в бурый цвет, обусловленный окраской NO2. Практически полностью диссоциирует при 140 °C. При увеличении давления при постоянной температуре степень диссоциации N2O4 уменьшается.
Так, равновесная концентрация NO2 при температуре кристаллизации (-11.2°C) в жидкой фазе составляет 0.01%, при температуре кипения (21.15°C) в жидкой фазе - 0.1%, в парах - 15.9%, при 135°C - 99%.
Чистый кристаллический N2O4 бесцветен, при загрязнении следами влаги окрашен в бледно-зеленый цвет, существует две аллотропных модификации - нестабильная моноклинная и стабильная кубическая.
Реагирует с водой с образованием смеси азотной и азотистой кислот:
Сильный окислитель, высокотоксичен и коррозивен. Смеси с органическими веществами взрывоопасны.
Получение
Образовавшийся NO2 при t=-8 °C переходит в жидкое состояние с образованием N2O4.
Применение
Широко применяется в ракетной технике в качестве высококипящего (некриогенного) окислителя ракетного топлива.
В ракетных двигателях используется в паре с топливами на основе производных гидразина (метилгидразином, несимметричным диметилгидразином), в Вооружённых силах РФ именуется «амил».
На начальном этапе использовался в виде раствора в азотной кислоте, из-за высокой температуры перехода в твёрдое состояние. В частности, на советских и российских РН «Космос», украинских «Циклон» (в виде АК-27И), «Протон»; американских — семейства «Титан»; французских — семейства «Ариан»; в двигательных установках пилотируемых кораблей, спутников, орбитальных и межпланетных станций. По степени использования стоит на втором месте после жидкого кислорода.
Тетраоксид азота в паре с алкилгидразинами образует самовоспламеняющуюся топливную пару с периодом задержки воспламенения около 0,003 с.
Хранение
N2O4 хранят в резервуарах из легированной стали или алюминия объёмом до 100 м³. Резервуары оборудуют сливно-наливными трубами, предохранительными клапанами, манометрами и уровнемерами. Поскольку интервал жидкого состояния при атмосферном давлении очень узок (262…294,3 К), резервуары размещают в заглублённых помещениях, где поддерживается температура 268…288 К.
В резервуарах поддерживается избыточное давление в 0,15—0,22 МПа для исключения попадания в окислитель из атмосферы влаги и загрязняющих веществ и для сокращения времени насыщения газами при заправке ампулизированных ракет. Заправленные ракеты также находятся под некоторым избыточным давлением, что исключает кавитацию в турбо-насосном агрегате (ТНА) при работе двигательной установки.
Транспортирование АТ
Тетраоксид азота транспортируют в специальных цистернах, имеющих изоляцию и систему трубопроводов, в которую в зависимости от температуры окружающего воздуха подают либо тёплую воду, либо охлаждающий раствор.
Транспортируется тетраоксид азота под избыточным давлением 0,1…0,15 МПа. Железнодорожные ЖАЦ-44, ЖКЦ-39 и автомобильные цистерны оборудуют сливно-наливными трубами, предохранительными клапанами, манометрами и уровнемерами. Железнодорожные цистерны имеют вместимость около 40 м³, автоцистерны — 30…60 м³. ОАО РЖД перевозит его в цистернах ЖАЦ-44.
См. также
Ссылки
- NIOSH Pocket Guide to Chemical Hazards: Азотный тетраоксид
Примечания
- ↑ В действительности, амил — это алкильный радикал C5H11. Название «амил» применительно к АТ — кодовое имя у военных ракетчиков.
- ↑ K. Jones. The Chemistry of Nitrogen: Pergamon Texts in Inorganic Chemistry
Данная страница на сайте WikiSort.ru содержит текст со страницы сайта "Википедия".
Если Вы хотите её отредактировать, то можете сделать это на странице редактирования в Википедии.
Если сделанные Вами правки не будут кем-нибудь удалены, то через несколько дней они появятся на сайте WikiSort.ru .


